医疗器械指令MDD分类规则
医疗器械指令(MDD)适用于有源植入式医疗器械指令或体外诊断医疗器械指令未涵盖的所有常规医疗器械。为了获得欧盟的医疗器械批准,必须对医疗器械进行正确分类。那么,医疗器械指令MDD分类规则是什么样的呢?

MDD根据风险和预期用途将产品分为不同类别,从而确定相关的合格评定程序。对于分类为中度至高度风险的产品(Is,Im,IIa,IIb和III类),《医疗器械指令》要求涉及指定机构的合格评定程序。
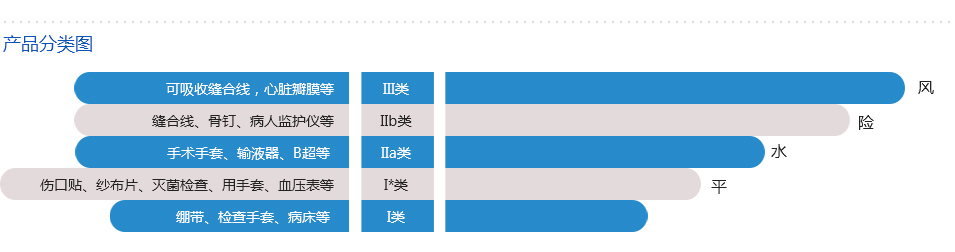
一、 产品分类规则
1、规则应用由器械的预期使用目的决定;
2、如果器械是和其它器械配合使用,分类规则分别适用于每种器械;
3、附件可以和其它一起使用的器械分开单独分类;
4、启动或影响某种器械的软件与器械属于同一类型。
二、分类准则
时 间: 暂时 (<60分钟)、短期(<30天)、长期(>30天)
创伤性:非创伤、通过孔径创伤,外科创伤 、植入。
适用位置:中央循环、中枢神经系统,其它地方。
能量供应:无源,有源。
规则1~4、所有非创伤性器械均属于I类,除非他们:
用于储存体液(血袋例外) II a类
于Ila类或更高类型的有源医疗器械类 II a类
改变体液成分 II a/II b类
一些伤口敷料 II a/II b类
规则5、侵入人体孔径的医疗器械
暂时使用(牙科压缩材料、检查手套) I类
短期使用(导管、隐形眼镜) II a类
长期使用(正常牙线) II b类
规则6-8、外科创伤性器械
再使用的外科器械(钳子,斧子) I类
暂时或短期使用(缝合针、外科手套) 11a类
长期使用(人工晶体) IIb类
与中央循环系统(CCS)或中枢神经系统接触的器械 III类
规则9、给予或交换能量的治疗器械 II a类
(肌肉刺激器、电钻、皮肤光疗机、助听器)一一种潜在危险方式工作的 IIb类(婴儿培养箱、高频电刀、超声碎石机、X光机)
规则10、诊断器械
提供能量 II a类
诊断/监视体内放射药物分布 II a类
(照相机、正电子发射成像仪)
诊断/监视生理功能(心电图、脑电图) II a类
危险情况下监视生理功能 II b类
(手术中的血气分析仪)
发出电离辐射(X射线诊断议) II b类
规则11、控制药物或其他物质进出人体的有源器械 II a类
(吸引设备、供给泵)
如以一种潜在危险方式工作 II b类
(麻醉机、呼吸机、透析机、高压氧舱)
规则12、所有其他有源医疗器械属于I类
(观察灯、牙科椅、轮椅、牙科用治疗灯、记录处理观察诊断图象用的有源器械)
规则13、与医用物质结合的器械(含杀精子的避孕套、含抗生素的牙髓材料) III类
规则14、避孕用具(避孕套、子宫帽 II b类 ), (子宫内避孕器 III类) III类
规则15、清洗或消毒的器械
医疗器械(内窥镜消毒) II a类
隐形眼镜清洗液 II b类
规则16、用于记录X射线图象的器械(X光片) II a类
规则17、利用动物组织的器械(生物)心脏瓣膜、肠线、胶原) III类
规则18、血袋 II b类
以上就是关于“医疗器械指令MDD分类规则”的相关内容,了解更多请咨询海外顾问帮。
【海外顾问帮】是协助国内企业和个人跨境发展一站式的服务中心,协同全球专家顾问,坚持透明服务,打破跨境壁垒,为医疗产品CE认证提供一站式服务,咨询电话: 400-106-2206。

医疗产品CE认证
直连专家
 邮件群发-邮件群发软件|邮件批量发送工具|群发邮件平台|批量邮箱发送系统公司
邮件群发-邮件群发软件|邮件批量发送工具|群发邮件平台|批量邮箱发送系统公司








